联芳基化合物不仅是众多手性配体、手性催化剂的核心骨架,而且也广泛存在于天然产物、药物活性分子以及材料领域中(图1a)。目前,化学家已经开发出多种方法来构建联芳基骨架(Nat. Chem., 2017, 9, 558),例如过渡金属催化的交叉偶联(图1b)、中心手性向轴手性的传递、联芳基化合物的去对称化及环加成等。然而,过渡金属催化的交叉偶联反应因底物预官能团化、多步合成、条件严苛等因素阻碍其选择性和连接性,致使四邻位取代联芳基骨架的构建仍然是有机化学领域的一大难题。此外,氧化偶联将两个C-H键转化成C-C键,为构建联芳基骨架提供了一种替代性策略(图1b),但是氧化偶联因底物自身固有的空间和电子特性,严重阻碍了其化学选择性、位点选择性和阻转选择性(图1c),并且该策略仅适用于富电子酚类底物,而缺电子酚的氧化偶联仍极具挑战性。另一方面,大自然已经进化出众多氧化酶,如漆酶和细胞色素P450酶,可介导酚类底物的二聚化以构建联芳基天然产物。然而,漆酶因自生选择性控制的缺陷,在选择性催化中的应用比较受限。相比之下,人们发现越来越多的P450酶可介导高选择性氧化反应,这些酶中的一小部分还可催化位点选择性和阻转选择性的二聚化反应。而这一部分具有氧化偶联活性的野生型P450酶,还尚未被用于催化非天然交叉偶联反应。
近日,美国密歇根大学(UMich)的Alison R. H. Narayan教授课题组利用细胞色素P450酶介导的生物催化策略(图1d),成功地实现了酚醛底物的氧化交叉偶联反应,构建了一系列联芳基化合物。通过定向进化,作者得到了一个具有高反应性、高位点选择性和阻转选择性的P450酶。这种构建空间位阻联芳键的生物催化策略,使得具有催化剂控制的反应性和选择性的可编程分子组装平台成为现实。相关成果发表于Nature 上。

图1. 氧化交叉偶联构建联芳基骨架。图片来源:Nature
首先,作者使用异源表达KtnC(一种细胞色素P450酶)的酿酒酵母进行了香豆素4的生物转化,可观察到二聚产物7的形成,但是酿酒酵母因为底物载量的限制不适合进行制备规模的反应。为了在酵母中开发可规模化反应的全细胞生物催化平台,作者将编码KtnC的基因整合到毕赤酵母中,使联芳基产物的总产率增加三倍以上,并实现了制备规模反应。有了优化的生物催化平台,作者尝试将二聚反应转向非天然的氧化交叉偶联化学(图2a)。他们认为酶活性位点可促进两种非等价酚类底物的结合,并克服有机小分子介导的氧化交叉偶联反应中传统的空间和电子限制等问题。事实上,将香豆素4和16添加到产生 KtnC 的培养物中,可形成非天然的交叉偶联产物。进一步筛选表明,调整交叉偶联底物的化学计量可获得交叉偶联为主的产物。在此基础上,作者利用KtnC 催化的交叉偶联反应策略,对一组香豆素底物进行了考察(图2b)。4与9-12间的初始交叉偶联反应表明,在 C4 和 C5 位置上保持与 4 相似的取代模式对反应是有益的,但并不从根本上影响活性。另外,KtnC 可耐受一系列带有富电子和缺电子取代基的香豆素(13-16),同时还能耐受C4 和 C5 位基团体积较大的香豆素(17-22)。需要指出的是,大多数交叉偶联反应保持其二聚反应中的位点选择性和阻转选择性(图2c)。例如,4 与18 间的交叉偶联反应以优异的阻转选择性获得8,8′-连接的产物(P)-23,同时还观察到少量罕见的 6,6'-连接的产物(P)-24。与丁酯(22)的交叉偶联则以2:5的位点选择性得到8,8'-产物(25,minor)和6,6'-产物(26,major),而传统的方法则无法构建6,6'-连接的骨架。此外,作者还将多样化的酚醛底物作为香豆素4的偶联体(图2d),并且观察到与4相似的酚类底物具有优异的反应性;而随着底物结构与天然香豆素骨架的差别越来越大,其活性和位点选择性均显著降低。
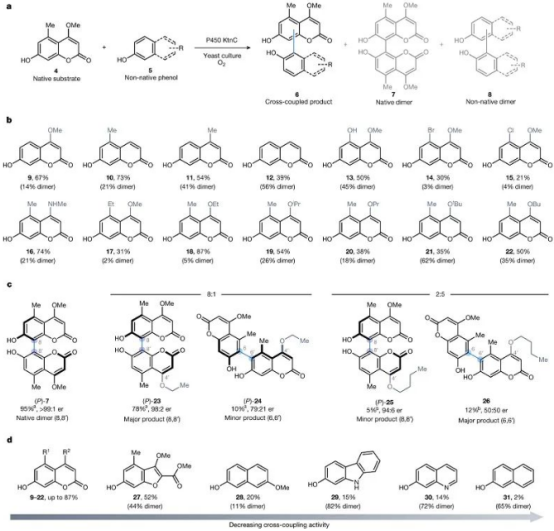
图2. 野生型KtnC催化氧化交叉偶联的底物范围。图片来源:Nature
其次,因野生型KtnC显示出较低活性和位点选择性(四种交叉偶联产物的总产率<3%),因此作者尝试通过定向进化策略来获得一种更高效的交叉偶联生物催化剂(LxC),从而将低产率、非选择性的反应转化为具有实用前景的合成方法(图3a)。具体而言,作者首先构建蛋白质文库,通过半理性诱变产生数千个变体,这些变体在野生型KtnC活性位点 12 Å 范围内具有一个或多个氨基酸残基替换。然后以香豆素 10 和 2-萘酚(31)为模型反应进行高通量筛选,并使用 Rapid-Fire 质谱(MS)分析交叉偶联产物的产率,产率较高的样品再进行LC-MS分析以判断其交叉偶联位点选择性。经过多轮迭代的定向进化,交叉偶联反应的总活性和位点选择性逐渐提高(图3c)。前两轮蛋白质工程中使总的交叉偶联产物产率增加了19倍,并保持较低的香豆素二聚化。然而,反应的位点选择性并不理想,C-O 键交叉偶联产物(35)将近占LxC2催化合成的所有交叉偶联产物的一半。后续的定向进化遂以提高工程酶的位点选择性为目标。经五轮迭代的定向进化,获得了一种活性提高了92 倍的生物催化剂LxC5,制备规模的生物转化也能以 50% 的分离产率得到目标产物32,远远高于传统合成方法。虽然产率和位点选择性的问题解决了,但遗憾的是,该反应的阻转选择性从80:20 er (野生型酶)降低至52:48 er (Lcx5)。为此,作者又进行了另外两轮定向进化以提高阻转选择性(图3d),并成功获得了理想的生物催化剂LxC7,后者能以77:23 er 得到目标产物32。上述结果表明,该生物催化平台的活性、位点选择性和阻转选择性都可通过蛋白质工程进行调控,从而为催化剂控制的氧化交叉偶联反应提供了一个可编程的平台。
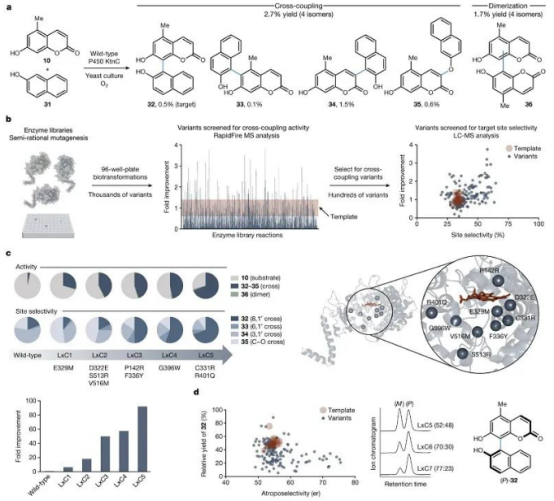
图3. 通过定向进化提高P450生物催化剂的活性和选择性。图片来源:Nature
在使用蛋白质工程策略的同时,作者认为还存在其他相关的野生型酶,可以作为氧化交叉偶联反应的补充催化剂。为此,作者采用生物信息学方法对可介导分子间氧化二聚化反应的酶序列进行了筛选分析,得到了可能催化与萘酚的氧化交叉偶联反应的酶。通过将P450RhF还原酶结构域(RhFRed)连接到每个P450的羧基末端来构造人工融合酶P450–RhFRed,以重建催化活性所需的电子传递。使用P450–RhFRed库进行筛选,作者发现了可使多种酚类底物与萘酚以1:1的比例形成交叉偶联产物的融合酶(图4b)。尽管不同的交叉偶联反应的产率有所不同(43-46),但这些转化有利于交叉偶联产物而不是竞争性的二聚体的生成,因而降低了一种底物对另一种底物大大过量的要求,提高了底物的化学选择性和位点选择性。总之,不同 P450 催化剂可实现互补反应性,为构建不同联芳基骨架提供了新的生物催化途径。
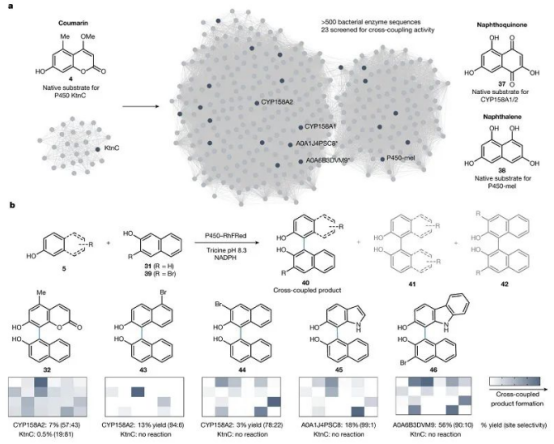
图4. 探索具有互补反应性的生物催化剂。图片来源:Nature.
总结
Narayan教授使用细胞色素P450酶催化酚醛底物的氧化交叉偶联反应构建联芳基骨架,并通过定向进化扭转野生型酶的低反应性及低选择性的不利局面。该方法不受底物空间和电子性质的限制,克服传统方法中底物反应性的障碍,并为催化剂控制的位点选择性和阻转选择性提供了新的机会。该方法不仅为构建联芳基化合物提供了一个高效、环保的方法,而且提供了一个具有催化剂控制的反应性和选择性的可编程分子组装平台。
文章来源:Biocatalytic oxidative cross-coupling reactions for biaryl bond formationLara E. Zetzsche, Jessica A. Yazarians, Suman Chakrabarty, Meagan E. Hinze, Lauren A. M. Murray, April L. Lukowski, Leo A. Joyce, Alison R. H. Narayan Nature, 2022, 603, 79–85, DOI: 10.1038/s41586-021-04365-7